已完成BE研究 两个仿制药上市申请拟优先审评
发表日期:2017-06-21
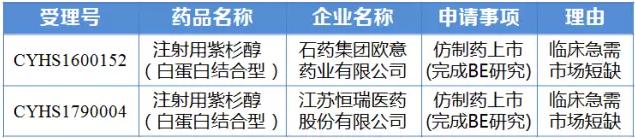
6月21日讯 6月20日,CDE官网公示了第二十批拟纳入优先审评程序的药品注册申请名单。涉及的品种是注射用紫杉醇(白蛋白结合型),分别是由石药集团欧意药业有限公司与江苏恒瑞医药股份有限公司提出的仿制药上市申请。值得注意的是,两家企业均已对该品种完成BE研究。
第二十批拟纳入优先审评程序药品注册申请公示名单
上一篇: 200亿眼科药市场抗青光眼新药当道:细看Top 5品种
下一篇: CFDA最新批准,100个医疗器械获准上市
热门文章排行
更多>>
- 联合国秘书长呼吁停止歧视自...
- 重庆居民慢性病自我管理组首...
- 医学期刊表现抢眼 我国学术...
- 2010年6个医学相关学科取得...
- 听障和脑瘫抢救性门诊费实现...
- 七部门联合检查 所有医疗机...
- 青岛联动机制智斗非法行医“...
- 湖北重点地方病防治“答卷”...
- 山西6月底前实现城镇医保市...
- 零差价冲击客源 单体药店或...
- 医学类毕业生就业冷热不均
- 医药职专就业:畅通“出口”...
- 上海五年内将对儿科、产科、...
- 硕士去绍兴就业 购房打6折
- 应届毕业生春季招聘进入倒计...
- 学历门槛成了就业拦路虎
- 县级医院发展势头猛 医疗人...
- 首批医疗监督大使给力民营医...
- 全球每年死产婴儿数降幅仅1....
- 卫生信息化发力 公私医院实...







